Aufgabe (BW03x001) *
Wann ändert sich die innere Energie eines idealen Gases nicht?
(Stichwortartig begründen!)
bei jeder isobaren Kompression
wenn sich der Druck bei konstantem Volumen erhöht
bei einer adiabatischen Zustandsänderung
bei einer isothermen Zustandsänderung
bei jeder Zustandsänderung ohne Zufuhr von mechanischer Arbeit
Lösung (BW03x001)
Keine Änderung der inneren Energie bei einer isothermen Zustandsänderung
Beim idealen Gas ist die Änderung der inneren Energie proportional zur Temperaturänderung.
Aufgabe (BW03x002) *
Drei Mol eines idealen zweiatomigen Gases nehmen bei der Temperatur 300 K und dem Druck p0 ein Volumen von 20 m3 ein. Wie groß ist der Druck, wenn das Gas adiabatisch bis 40 m3 expandiert?
$p_0\cdot\left(\frac{1}{2}\right)^\frac{1}{2} $
$p_0\cdot\left(\frac{1}{4}\right)^\frac{7}{5}$
$p_0\cdot\left(2\right)^\frac{7}{5}$
$p_0\cdot\left(4\right)^\frac{5}{3}$
$p_0\cdot\left(\frac{1}{2}\right)^\frac{7}{5}$
Lösung (BW03x002)
$p_0\cdot\left(\frac{1}{2}\right)^\frac{7}{5}$
$p^\prime\ {V^\prime}^\kappa=p_0 {V_0}^\kappa$
$c_V=\frac{5}{2}R\ \Rightarrow\ \kappa=\frac{7}{5}\ $
Aufgabe (BW03x004) *
Ein Autoreifen ist im Sommer bei 20°C mit einem Überdruck von 3,0⋅105 Pa aufgepumpt. Wie groß ist der Überdruck bei 0°C ? (Die Reifengröße soll als unverändert und der Atmosphärendruck als konstant 1,0⋅105 Pa angenommen werden.)
4,0⋅105 Pa
3,0⋅105 Pa
2,8⋅105 Pa
1,78⋅105 Pa
1,6⋅105 Pa
Lösung (BW03x004)
$\frac{p_1}{T_1}=\frac{p_2}{T_2}$
2,8⋅105 Pa
Aufgabe (BW03x006) *
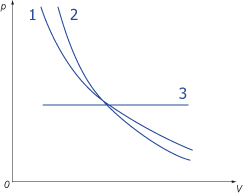
In dem nebenstehenden p-V-Diagramm sind die Kurven 1, 2 und 3 eingezeichnet. Die eine ist eine Isotherme, die andere eine Adiabate. Welche ist die Isotherme, welche die Adiabate? Um welche Zustandsänderung geht es in der dritten Kurve?
1: Adiabate; 2: Isotherme ; 3: Isobare
1: Isotherme; 2: Adiabate; 3: Isobare
1: Isotherme; 2: Adiabate; 3: Isochore
1: Isochore; 2: Isotherme; 3: Adiabate
1: Adiabate; 2: Isobare; 3: Isotherme
Lösung (BW04x006)
1: Isotherme; 2: Adiabate; 3: Isobare
Adiabate "steiler" da:
Isotherme: $p\cdot V=const.$
Adiabate: $p\cdot V^\kappa=const.$
Isobare: Druck konstant
Aufgabe (BBW02x002) *
Zwei Flüssigkeiten (gleiche Substanz) werden in einer Thermoskanne gemischt. Die Flüssigkeit mit der höheren Temperatur(60°C) hat die doppelte Masse wie die kältere Flüssigkeit (30°C). Die Mischtemperatur beträgt:
35°C
40°C
45°C
50°C
55°C
Lösung (BW02x002)
$c\ m\ ( T_1-T ) = c\ m\ ( T-T_2 );$
Mischtemperatur: 50°C.
Aufgabe (BW03x005) *
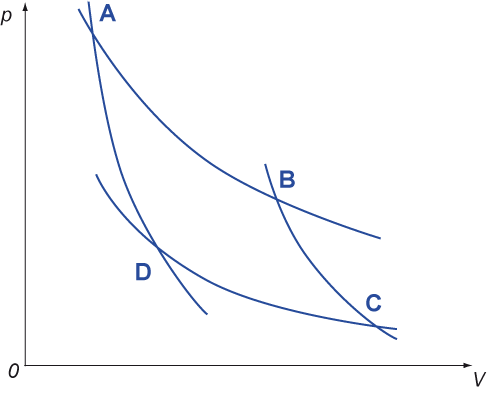
In dem gezeigten Kreisprozeß sind AB und CD Isothermen, DA und BC Adiabaten. Ein System durchläuft den Carnot-Prozeß ABCD, nimmt die Wärmemenge $Q_2$ aus dem Reservoir mit $T_2$ auf und gibt die Wärme $Q_1$ an das kältere Reservoir mit der Temperatur $T_1$ ab. Kreuzen Sie die 3 richtigen Aussagen in der nachfolgenden Liste an.
Die Entropie des Systems nimmt zu.
$Q_1/T_1=Q_2/T_2$
Die Entropie des wärmeren Reservoirs nimmt ab.
Die verrichtete Arbeit ist gleich der Netto-Wärmeaufnahme $Q_2-Q_1$.
Der Wirkungsgrad des Kreisprozesses hängt von der Arbeitssubstanz ab.
Lösung (BW03x005)
$Q_1/T_1=Q_2/T_2$
Die Entropie des wärmeren Reservoirs nimmt ab.
Die verrichtete Arbeit ist gleich der Netto-Wärmeaufnahme $Q_2-Q_1$.
Aufgabe (BW06x001) *
Die Stahlungleistung eines schwarzen Körpers beträgt 10 mW bei der Temperatur $T_1$. Wie groß ist seine Stahlungsleistung bei der Temperatur $T_2 = 2\ T_1$? (Stichwortartige Begründung!)
60 mW
100 mW
120 mW
160 mW
180 mW
Lösung (BW06x001)
Die Leistung beträgt 160 mW.
Stefan-Boltzmannsches Gesetz: $P\ \sim\ T^4 $.